依頼者向け説明資料
DDworks21/Trial Siteシステム概要(紹介及び機能説明)(2019.12)
依頼者様向け操作の説明(2021.10)
DDworks NX/Trial Siteへの移行に伴う説明資料(2021.07)
*2021年秋以降に開始する試験のうち“依頼者側Exchangeと連携する試験(以下、連携申請)”に
ついて、当院では安全性情報の一括交付先に治験責任医師は含まれておりません。
また、連携申請の有無に関わらずTrial Siteを介した治験責任医師への文書交付・安全性情報の
見解確認は行わないでください。
ユーザーズガイド(初回ログイン時はこちらをご覧ください。)
*システムのURLはユーザーズガイドに記載されています。
Windowsの方はMicrosoft Edge又はGoogle Chromeを利用してください。
(Internet Explorerは利用不可)
Customer ID:okayama-u Logon ID:各個人メールアドレスの@前です。
(システムよりメールで通知されます)
ログイン後、ユーザーズガイドに従ってPCのセットアップを行ってください。
システム化業務フロー
SDV・監査の際の操作手順
アカウント発行申請書
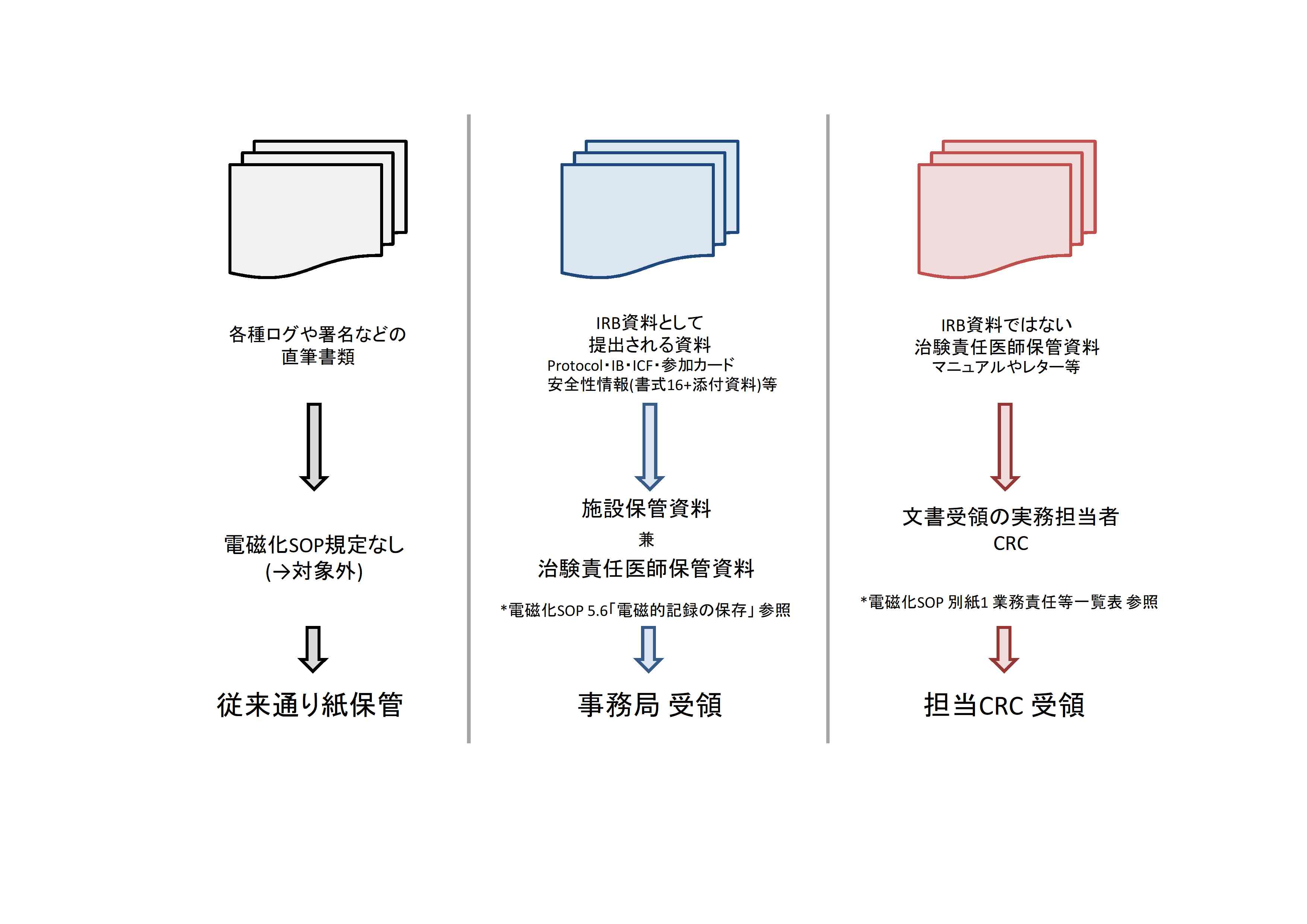
資料の提出先及び取扱いについて
当院の電磁化SOP5.6に
「IRB資料として提供された資料は責任医師保管分として共用する」
という旨の記載があります。
当院ではこの運用を適用しているため、
安全性情報の治験責任医師保管分として治験責任医師宛にシステム内で交付いただく必要ありません。
ただし、見解確認のために提供は必要かと思いますので、
これまでと同様の方法(紙・メール・依頼者様独自のシステム等)で御提供ください。
また、担当CRC宛にマニュアルやレター等の治験責任医師保管資料を交付する際には、
必ず件名に【責任医師保管資料】と用件を明記してください。
電磁化標準業務手順書及び電磁化チェックリストは標準業務手順書/書式ページに公開しております。
※チェックリストの内容確認・署名等は事務局が対応します。事務局(irbdesk@okayama-u.ac.jp)宛にメールでご連絡下さい。

